外部寄稿
バイオエコノミーやバイオトランスフォーメーション(BX)という概念が広まりつつある。いずれもバイオテクノロジーをテコに社会や経済を改善しようというものである。本稿では、バイオテクノロジーの進展が社会・経済にもたらすインパクトやその推進における産学官の役割について、バイオテクノロジーの開発と普及という観点から、経済学的に検討する。またBXの守備範囲は広範にわたるため、ここでは健康・医療分野に焦点を絞る。
バイオテクノロジーとは、生物学(Biology)と技術(Technology)の造語であり、生物の持っている働きを人々の暮らしに役立てる技術、とされる(経済産業省, 2024)。その対象は健康・医療、エネルギー、食糧、環境など広範にわたっている。このバイオテクノロジーを軸に、近年“バイオエコノミー”という言葉が浸透しつつあった。2009年にOECDが発表したレポートによると、近年の世界が直面する環境・社会・経済的課題に対して、バイオテクノロジーが技術的解決策を提供し、特に一次生産、健康、産業に応用されることで、バイオテクノロジーが経済生産の大きな割合を占める「バイオエコノミー」が出現しうるという(OECD, 2009)。日本ではバイオエコノミーを、バイオテクノロジーとバイオマス(生物由来の有機物)を活用した循環型の、持続可能な経済社会と解釈することが多いようである。日本でも2019年に「バイオ戦略」が策定され、2024年には「バイオエコノミー戦略」と改称された(令和6年6月統合イノベーション戦略推進会議決定)。これは日本の強みを活用してバイオエコノミー市場を拡大し、諸課題の解決と持続可能な経済成長を両立しようとするものである。
それに対して産業界の側から提言されたのが“バイオトランスフォーメーション(BX)”戦略である。これは一般社団法人日本経済団体連合会(経団連)が、デジタルトランスフォーメーション(DX)、グリーントランスフォーメーション(GX)に続く第三の変革として提唱したものであり、バイオテクノロジーを活用して、社会課題の解決と持続可能な経済成長を両立しようという取り組みである(2023年3月10日)。さらに上述のバイオエコノミー戦略の策定に先駆けて、工業・エネルギー、食糧・植物、健康・医療分野を対象に個別重要施策を提言した。
このように官民挙げて、バイオテクノロジーを軸に持続可能な経済成長と社会課題の解決を図ろうとしている。技術革新は経済成長のエンジンである。技術革新は生産効率を上げ、これまでにない製品・サービスを生み出すことを通じて新たな市場を作り、富の拡大に貢献してきた。一方で、急速な経済成長は環境破壊や資源の枯渇など思わぬ副作用をもたらしてきた。これに対して、バイオエコノミー戦略やBX戦略がめざすものは、ともすればトレードオフを起こしがちな(持続可能な)経済成長と社会課題解決の両立を図ろうというものであり、経済学的にみれば大きなチャレンジであり、実現できれば社会・経済にもたらすインパクトは大きいものと考えられる。
ここでいま一度、なぜ基礎研究が政府主導で、また大学・公的研究機関によって担われるか、その理由について、経済学的に整理する。画期的な技術の開発には、基礎研究の成果が不可欠である。特にバイオテクノロジーの場合、生命科学の基礎研究の成果に負うところが大きい*1。企業のみで基礎研究を十分な水準まで行うことは難しい。基礎研究は科学的な知識を生み出す作業である。知識は無形の資産であり、誰が利用しても減るわけではなく(非競合性)、その利用を妨げることもできない(非排除性)という意味で”公共財”といわれる。公共財は誰しも自由に利用できてしまうため、開発企業が基礎研究から得られる利益を専有することは難しく、研究開発費を回収できなくなる。そのため、基礎研究をもっと行った方が、社会全体の利益が大きくなるとしても、企業は十分に基礎研究を行えない。また基礎研究は、成果につながるまで長い時間を有し、実際にどのような成果につながるか、不確実性が高い。こうした大きな不確実性を伴う基礎研究を、企業のみで行うことは困難であり、市場メカニズムに任せておけば、基礎研究の水準は、社会的に望ましい水準よりも過少になる。そこで市場メカニズムとは独立して、政府による公的資金を受けて、大学・公的研究機関が基礎研究の中心的な役割を担うことになる。無論、そこで生み出された知識は、産学連携あるいは非公式の経路を通じて、産業側に移転される必要がある。
大学・公的研究機関から科学的知識が産業側に移転されたとして、技術、製品サービスの研究開発においては、民間企業が果たす役割が大きい。企業は市場を通じて消費者のニーズをとらえることができ、ニーズを踏まえた製品・サービスを生み出すことで、消費者の厚生を改善することに寄与する。
しかし、健康・医療分野、特に医薬品については、他の製品・サービスの開発以上に、制度や規制によって研究開発が制約される面が大きい。規制が厳しいのは、どの国も同じであるが、規制当局の支援には違いがある。例えば、米国ではFDA(Food and Drug Agency)が医薬品の創出に研究開発段階から積極的に関与し、企業と共同して進めるのに対して(安積他、2005)、日本では規制当局がそこまで関与することはなく、臨床研究も含め企業任せの部分が大きかった。ただし、COVID-19パンデミックを経て、独立行政法人医薬品医療機器総合機構(PMDA)が、早期の臨床試験のために必要な試験・治験計画策定、開発計画などへの助言を行うスキームを開始するなど(2020年10月)、改善の兆しはある。
また治験環境も企業の研究開発に影響する。1997年に医薬品の臨床試験の実施に関する基準(Guideline for Good Clinical Practice: GCP)が新たに公布され、以前とは違い、医師のみで治験が実施しづらくなり、さまざまな手続きが必要になった。加えて、医薬品承認における外国臨床データの受け入れの拡大といった規制緩和や、国内治験の手続きの煩雑さへの不満からの海外治験への移行もあり、国内治験の件数が急減した(楠岡, 2018)。もともと日本は充実した皆保険制度があり、皆が低廉で、高品質の医療を受けることができるため、治験に参加するインセンティブが低く、大規模な治験を行うことが難しい。しかし、来たるゲノム創薬やテーラーメイド医療の実現など、創薬環境の変化を見越して、治験実施体制の強化を意図して、2003年から「全国治験活性化3カ年計画」が実施され、2007年には「新たな治験活性化5カ年計画」、2012年に「臨床研究・治験活性化5か年計画2012」が策定された。その後は新たな活性化計画はなく、臨床研究・治験の推進に関する今後の方向性が示されるのみのようである(厚生科学審議会臨床研究部会, 2019)。
このように20年以上前からバイオ医薬品開発の進展を予見して治験環境の整備は検討されてきたが、新型コロナ感染症ワクチンの開発の遅れにもみられたように課題は多い。治験環境の整備については、経団連、すなわち企業側からも具体的な提言がされている(上述のBX戦略内)。治験環境の影響を受けるのは開発を担う企業であるため、その整備は産官が連携して検討していく必要があろう。
バイオテクノロジーの進展は、これまでの既存の制度を根本から変える可能性がある。例えば遺伝子診断により、同一の病気であっても患者間での差異を踏まえた適切な医療を提供できるようになり(テーラーメイド医療)、副作用の防止や発症予防によって医療費削減に貢献しうる。一方で、保険のメカニズムは不確実性が存在する場合に機能する。すなわち、どのような疾病に罹患(りかん)するかわからない不確実性のある状態で、事前に保険料を払うことで、罹患した場合の医療費を負担するというリスクを保険会社に引き受けてもらう、というのが保険の仕組みである。しかし、遺伝子診断により、個人の疾病リスクなどがある程度識別・予想できるようになれば、少なくとも民間の保険会社はリスクの高い人を引き受けないため、高リスク者が保険市場から排除される可能性がある。極論すれば、限りなく不確実性が低減されるなら、保険市場そのものが機能しなくなる。このようにバイオテクノロジーの進展は、これまで機能していた既存のシステムも変えうる。この場合、保険市場にゆだねれば、高リスク者が保険に入れないという公平性の問題や、さらには保険市場自体の機能不全を起こしうるため、政府はより公的医療保険制度の機能を強化する必要が生じるだろう。
上述のテーラーメイド医療により医療費削減の可能性はあるが、医療経済学において有名な説は、医療費増加の最たる要因は医療技術の進歩に由来する、というものである(Newhouse, 1992)。実際、近年、1件当たりが高額な医療技術が次々に登場している。例えば画期的な白血病等治療薬「キムリア」の当初の薬価は患者1人当たり3,349万円ほどであった(2019年)。脊髄性筋萎縮症の遺伝子治療薬である「ゾルゲンスマ」の薬価は当初、患者1人当たり1億6,707万円ほどであった(2020年)。ただ、これらの対象となる患者数はそれほど多くはないため、保険財政への影響は限定的である。しかし、より患者数の多い疾病に高額な医療技術が適用された場合、その限りではない。その例が世界初の免疫治療薬「オプシーボ」である。2014年に保険承認されたときの薬価は約73万円/100mgであり、患者1人当たりの年間の薬価は約3,800万円であった。当初はメラノーマにのみ適応されたが、2015年12月に肺がんも対象となった。肺がん患者数は多いため(年間12万人超)、73万円という薬価では医療保険財政が破綻しかねないということで、緊急で2017年2月に薬価が改定され、半額ほどに引き下げられた。通常、薬価改定は2年に1度であるため、これだけでも異例のことであったが、その後も再算定が複数回行われる事態となった。そこで2019年から新薬価ルールとして、費用と効き目のバランスを吟味する費用対効果評価の制度を本格的に導入することとなった。
日本では安全性、有効性が確認された医薬品は、保険収載されることが前提である。画期的な医薬品は高額になりやすいが、薬価を引き下げることで対応しようとすれば、企業の開発インセンティブをそぐことにもなり、イノベーションの阻害要因になる。これに対して、いずれは保険収載を前提に、まずは保険外で運用し、保険診療との併用を認める「保険外併用療養費」で柔軟に対応することも検討されているが、保険外の部分が恒久化することに対しては、所得の多寡による高度な医療へのアクセス格差が生じうることから、公平性の点で強い反発がある。
バイオテクノロジーの進展はめざましく、これからも画期的な新薬が開発されることが予想されるが、新しい医療技術ができても医療保険制度の整備が追い付かなければ普及しない。高額な医薬品をどう保険収載するかは、保険財政の問題もさることながら、医療アクセスの公平性という観点もあり、これらと整合的な医療保険制度の設計をしなければ、バイオ医薬品の開発や普及にも影響するだろう。科学技術振興と医療保険制度は整合的に設計されなければならない(齋藤, 2014, 2015)。
バイオテクノロジー関連の開発においては高度知識人材が必要である。特にバイオテクノロジーは基礎研究が重要であるため博士人材が必須となり、人材育成の点で大学の果たす役割は大きい。しかしながら、図1で示すように、博士人材は減少もしくは停滞の一途を示している。
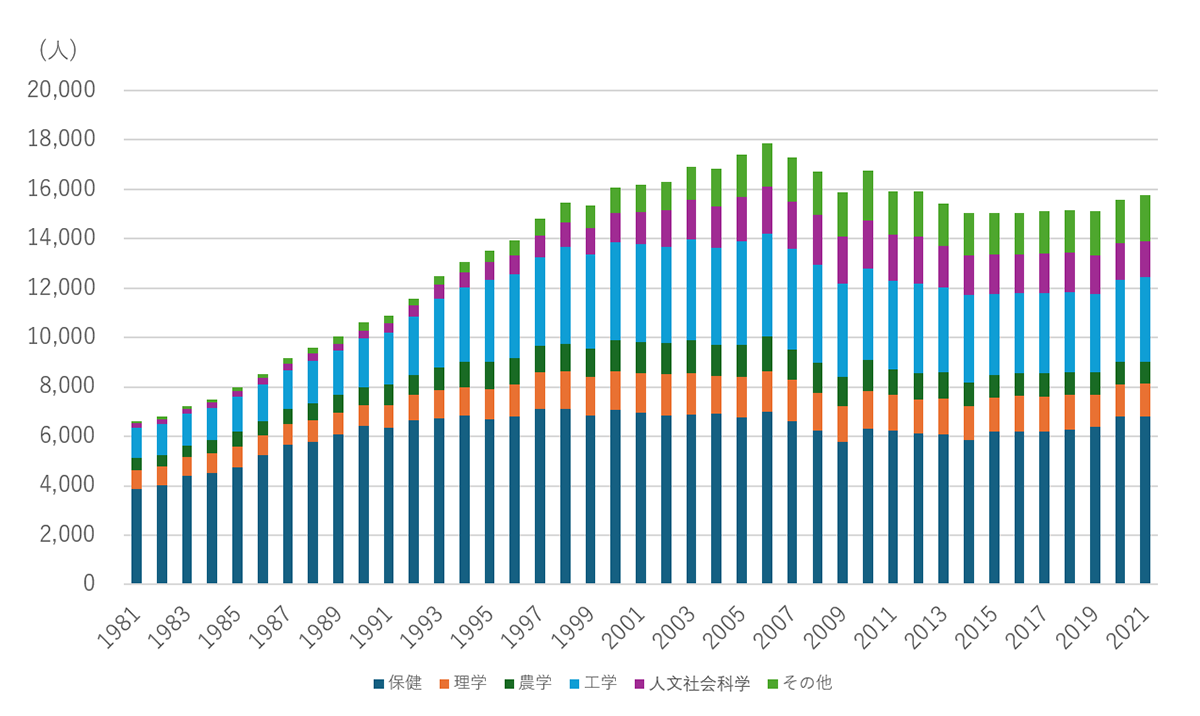
出典:科学技術指標2024に基づき筆者作成
図1 日本の博士号取得者数推移(主要専攻別)
図1は日本の博士号取得者(主要専攻別)の推移を示したものであるが、全般的に2000年代中ごろから低下もしくは停滞している。バイオとの関連が強い保健、理学、農学でみても、長きにわたり停滞、低下傾向にある。そもそも日本は先進諸国に比べて、博士号取得者が少ない(図2)。
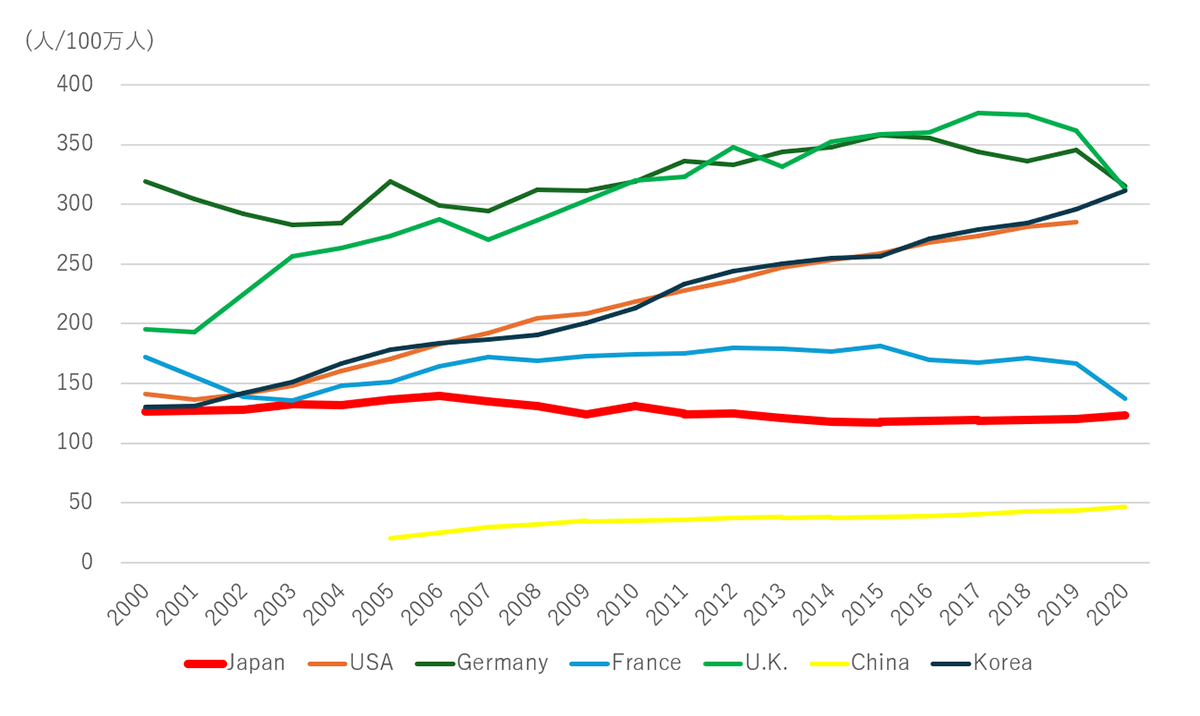
出典:科学技術指標2024に基づき筆者作成
図2 主要国の博士号取得者数(100万人当たり)推移
図2は主要7カ国の100万人当たり博士号取得者数の推移をみたものであるが、中国を除き、他国に比べて日本は常に低水準・定常にある。米国、ドイツ、英国、韓国は上昇傾向が続き、特に英国・ドイツは常に高水準である。
博士号取得者の減少・停滞は、博士課程進学者の減少・停滞を反映しているものと考えられるが、その背景には、長く繰り返されてきた博士労働市場の不均衡の問題がある。歴史的な経緯の詳細については長根(2021)、長根(2024)を参照されたいが、1970年代から断続的に博士号取得者を増やす政策が行われ、教員ポストを上回るスピードで博士号取得者が増えた結果、職に就けない者を生んできた。無論その都度出口戦略としてポスドク制度の創設や、多様なキャリアパスの推進なども行われたが、博士号取得者の供給を上回るほどにその需要は増えず、博士労働市場の不均衡を生んだ。そもそも、博士号取得者のキャリアパスとしてはアカデミアのみならず産業界も考えられるが、企業側の博士号取得者の採用は進まなかった。
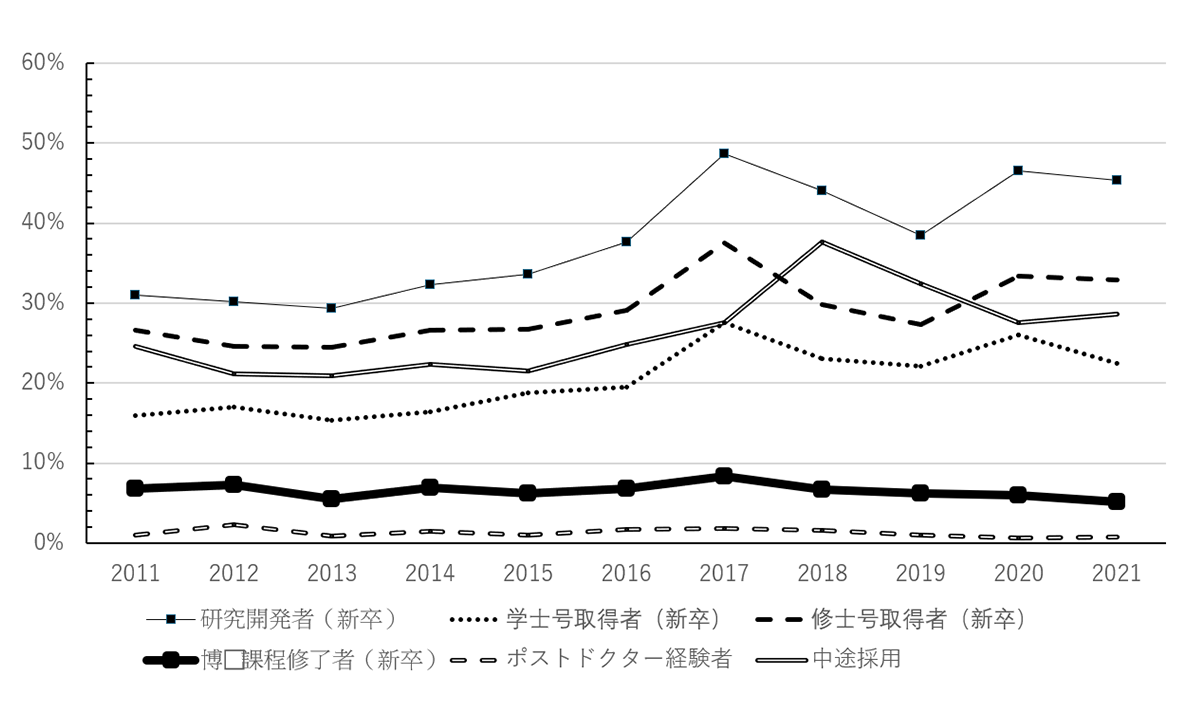
出典:科学技術・学術政策研究所、民間企業の研究活動に関する調査報告 2022 に基づき筆者作成
図3 学歴・属性別 研究開発者を採用した企業割合の推移
図3は、研究開発者を採用した企業の割合の推移であるが、博士課程修了者を採用する企業の割合は、修士や学士の学生を取得する企業割合に比べて著しく低い。無論、産業分野によって博士号取得者の採用割合は異なる。
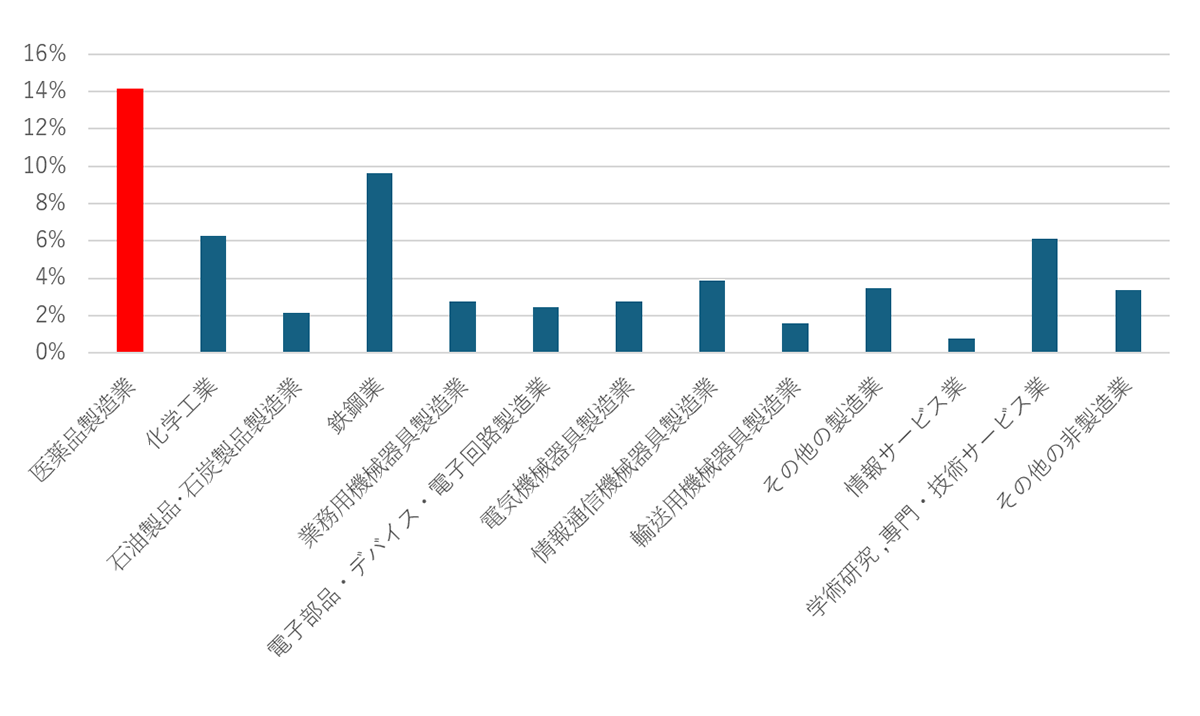
出典:科学技術指標2024に基づき筆者作成
図4 産業別 企業の新規採用研究者に占める博士号保持者割合(2022年時点)
図4は産業別の企業の新規採用研究者に占める博士号保持者割合であるが(2022年時点)、サイエンス型産業である医薬品製造業は最も高い。しかしながら、それでも14%程度である。このようにアカデミアでも、産業界でも博士号取得後のキャリアパスが描けない状況をみれば、博士課程進学者が減ることは当然だろう。
これに対して最近、政府は「博士人材活用プラン~博士をとろう~」を発表した。この大目標は2040年における人口100万人当たりの博士号取得者数を世界トップレベルに引き上げる(2020年度比約3倍)、というものであり、その中では多様なキャリアパスの構築の一環として、産業界とのマッチング支援のほか、官公庁や国際機関、起業家などでの活躍を支援する、としている。同時に、産業界に対しては博士人材の採用拡大や処遇改善に向けた協力をお願いする文書を公表している。
しかしながら、あくまでお願いベースであり、強制できるわけでもない。重要なのは、企業に対して博士人材の活用を促すことだけではなく、高度知識人材が求められるような市場を作り出すこと、すなわち、企業が博士人材を必要とするような高度知識に基づく新たな産業を形成することではないだろうか。その場合、企業側としても博士人材を採用することで、おのずから基礎研究の知識を吸収できることになる。バイオトランスフォーメーションは、そうした高度知識を必要とする産業を作り出す契機にもなるし、そうなるように産学官挙げて展開していく必要があるだろう。
技術進歩は国民の厚生を改善することを目的としているが、未知の医薬品をめぐっては国民の不安も大きい。ワクチンをケースに挙げると、例えば新型コロナワクチンを巡っても、その副作用や効果を巡り、国民の中に一定の不安があった。もともと日本ではワクチンに対する信頼度が低く、ある調査によれば149カ国中最低との結果も報告されている(Figueiredo, et al. 2020)。
多くの一般国民は、ワクチンなど医薬品に関する専門的な情報もなければ、情報があったとしても理解するのも難しい。一般国民と政府・製薬企業・医療従事者の間には“情報の非対称性”があり、情報量もそれを読み解くリテラシーも後者が優位である。そうなれば一般国民は政府など情報優位な主体が発信する情報を信じるしかないが、政府も因果関係をはっきり証明できない場合、人間は危険回避的な傾向があるためワクチン接種に慎重にならざるを得ない(長根, 2023)。またワクチンによって感染者や死者を減らす効果が大きくても、健康被害の方が大きく報道されがちであればなおさらである。このように、新しい未知の医薬品をめぐる国民の不安は尽きない。最近でも新しい新型コロナワクチンとして登場したレプリコンワクチンを巡り、接種者から非接種者に感染するのではないか、という懸念が日本看護倫理学会から表明されたことなどもあり(日本看護倫理学会, 2024)、不安が伝播し、レプリコンワクチン接種者の入店を断る動きも出た。
情報の非対称性がある以上、未知の技術に国民が不安を覚えるのは当然である。政府、企業は十分な情報提供と説明をしなければならない。また技術のもとになる科学的知識の国民向けの説明は、大学がアウトリーチ活動の一環として担うことも必要であろう。
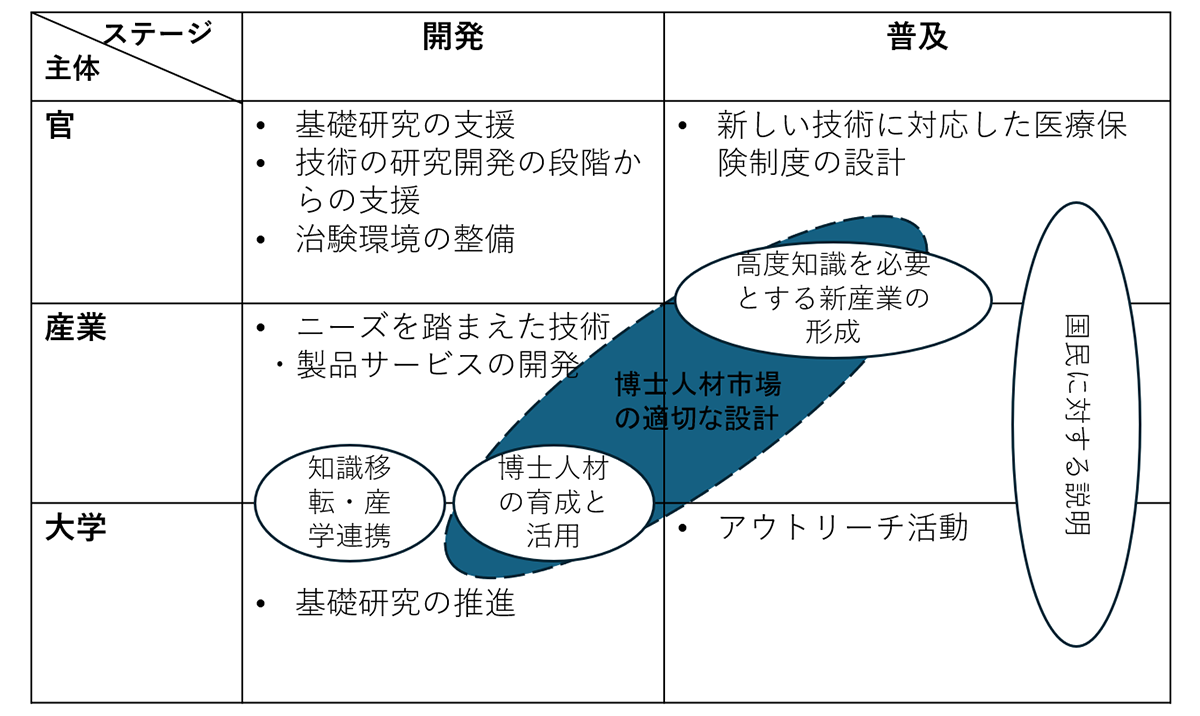
図5は、本稿の議論を踏まえて、バイオトランスフォーメーション推進における産学官の役割を、開発と普及という観点に分けて整理したものである。
出典:筆者作成
図5 バイオトランスフォーメーション推進に係る産学官の役割
バイオテクノロジーの開発と普及は一体的に行われなければならない。どちらか一方が先行してもだめで、例えば医療技術の開発だけ先行しても、それを経済的に利用可能にする医療保険制度の整備が伴わなければ画期的な医療技術も普及せず、社会にインパクトをもたらすことはない。また大学側がいくら高度知識人材を育成したとしても、それを産業側が取り込まなければ、高度知識の移転は進まず、新たな産業形成にもつながらない。開発と普及の一体的な推進のためには、産学官の協働が重要である。
謝辞
本論文は、科研費(22H00835)および日本証券奨学財団の助成による研究成果を含む。記して感謝したい。

長根(齋藤) 裕美(ながね(さいとう) ひろみ)
千葉大学大学院 社会科学研究院 教授
博士(経済学)
専門:医療経済学、科学技術政策、イノベーションの経済学
政策研究大学院大学(GRIPS)助教授などを経て、現職。このほか、文部科学省科学技術・学術政策研究所客員研究官、GRIPS客員研究員、UCLA visiting scholarのほか千葉県、千葉市を中心に地方自治体の委員歴任。医療分野を中心に、技術の創出(研究開発システム)と普及(医療保険制度)の両面から研究。最近のテーマは「日本の研究力低下」「孤立・人間関係の多様性と健康」
執筆者紹介

長根 裕美
千葉大学大学院
社会科学研究院
教授
機関誌「日立総研」、経済予測などの定期刊行物をはじめ、研究活動に基づくレポート、インタビュー、コラムなどの最新情報をお届けします。
お問い合わせフォームでは、ご質問・ご相談など24時間受け付けております。